Amineoxide


Een amineoxide is een chemische verbinding met de algemene formule (R1R2R3)N+-O−; dit wordt soms ook geschreven als (R1R2R3)N→O en vroeger ook, maar foutief, als (R1R2R3)N=O. Een amineoxide bezit dus een stikstof-zuurstofbinding en drie, al dan niet identieke, organische groepen verbonden aan het stikstofatoom.
Veelgebruikte amineoxiden zijn pyridine-N-oxide en N-methylmorfoline-N-oxide.
Synthese
Amineoxiden worden bereid door de oxidatie van tertiaire amines of van pyridinederivaten, met behulp van een geschikte oxidator:
- Waterstofperoxide
- Perzuren, zoals perazijnzuur of m-CPBA
- Kaliumperoxosulfaat
- tert-butylhydroperoxide
Reactiviteit en eigenschappen
Amineoxiden zijn zeer polaire moleculen door de aanwezigheid van formele ladingen. Het zijn zwakke organische basen. Kleine amineoxiden zijn zeer hydrofiel en goed oplosbaar in water.
Toepassingen
Amineoxiden worden gebruikt als beschermende groep voor amines en als intermediair bij organische syntheses. Enkele reacties met amineoxiden zijn:
- de Cope-eliminatie, dit is de splitsing van amineoxiden door verhitten
- de reductie tot de corresponderende amine, met gebruikelijke reductiemiddelen zoals lithiumaluminiumhydride of natriumboorhydride
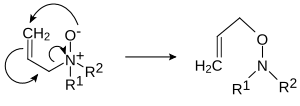
- de Meisenheimer-omlegging van een allylisch amineoxide tot een alkoxyamine:
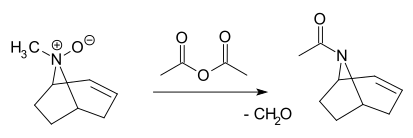
- de Polonovsky-omlegging van een amineoxide met azijnzuuranhydride of acetylchloride. Het amineoxide wordt gesplitst in het corresponderende aceetamide en een aldehyde:
Amineoxiden met één lange en twee korte alkylgroepen worden gebruikt als oppervlakte-actieve stoffen.