Muschio bianco
Il muschio sintetico, conosciuto principalmente come muschio bianco, nell'industria della profumeria è una classe di aromatizzanti sintetici, creati dalle aziende per emulare il profumo del cervo muschiato o di altri muschi naturali. Il muschio sintetico ha un odore pulito, morbido e dolce, privo delle note connotate alla natura animalesca del muschio originale, a cui a volte sono attribuite note di mora, ambretta o ambra grigia. Questi composti sono molto usati in cosmetici, detergenti, profumi e cibi, e formano le note di base nelle formule di numerose fragranze in commercio.[1][2][3]
Le principali sostanze chimiche responsabili dell'odore del muschi naturali sono i chetoni macrociclici muscone e civetone, presenti rispettivamente nel mosco nello zibetto. Nel tentativo di replicarne l'odore sono stati sono stati sviluppati i muschi sintetici. Nel tempo sono state sintetizzate strutture chimiche di tipo differente, che vengono in genere suddivise in quattro gruppi principali: muschi nitroaromatici, muschi policiclici, muschi macrociclici, e muschi aliciclici.[4] I primi due gruppi hanno trovato ampio utilizzo nell'industria, dalla cosmetica ai detergenti. Tuttavia, la rilevazione di composti dei primi due gruppi in campioni umani e ambientali,[5][6][7][8] nonché le loro proprietà cancerogene, ha avviato un dibattito pubblico sull'utilizzo di questi composti, e ha portato a un divieto o una riduzione del loro uso in molte regioni del mondo.[9] La ricerca ha indicato che questi composti non si disperdono nell'ambiente, possono accumularsi nel corpo umano, e possono abbattere le difese immunitarie contro le altre esposizioni chimiche tossiche. I composti di muschio macrociclici e aliciclici, ritenuti più sicuri, dovrebbero in futuro sostituire i primi due gruppi.[4]
Muschi nitroaromatici
Il primo muschio artificiale, noto come muschio Baur, fu ottenuto casualmente da Albert Baur nel 1888 mentre svolgeva ricerche su nuovi esplosivi alchilando il trinitrotoluene.[10] In seguito Baur ottenne anche i composti muschio xilene, muschio chetone e muschio ambrette che dominarono il mercato dei profumi per 50 anni.[2] Altri muschi nitroaromatici importanti introdotti in seguito furono il moskene (1930) e il tibetene (1935). La presenza del sostituente nitro provocava tuttavia problemi di instabilità in ambiente alcalino e in presenza di luce, e gli studi si volsero alla ricerca di composti muschiati senza sostituenti nitro. Negli anni 90 del secolo scorso l'uso di muschi nitroaromatici è andato declinando, e l'Unione Europea ha vietato l'impiego in cosmetica della maggior parte di questi composti. Solo il muschio chetone è ancora in uso in quanto risultato tossicologicamente innocuo.[1][11]
-
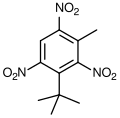 Muschio Baur
Muschio Baur -
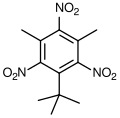 Muschio xilene
Muschio xilene -
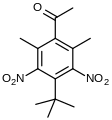
-
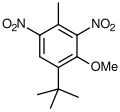 Muschio ambrette
Muschio ambrette -
 Muschio moskene
Muschio moskene -
 Muschio tibetene
Muschio tibetene
Muschi policiclici
La ricerca di muschi sintetici senza sostituenti nitro portò nel 1951 al fantolide, capostipite della nuova famiglia dei muschi policiclici. Successivamente apparvero versalide (1953), poi ritirato dal mercato per problemi di tossicità, tonalide (1954), celestolide (1955), galaxolide (1962), traseolide (1977) e vulcanolide (1989). I composti con maggior successo commerciale furono galaxolide e tonalide; nel 1997 ne furono prodotte rispettivamente 3800 e 1500 tonnellate.[12] Alla fine degli anni 90 i muschi policiclici costituivano circa il 75% del mercato dei muschi. In seguito l'uso dei muschi policiclici iniziò a declinare per problemi di bioaccumulo e biomagnificazione.[2]
-
 fantolide
fantolide -
 versalide
versalide -

-
 celestolide
celestolide -

-
 traseolide
traseolide -
 vulcanolide
vulcanolide
Muschi macrociclici
Nel 1926 Leopold Ruzicka riuscì a determinare la struttura macrociclica di muscone e civetone, due muschi di origine naturale, risultato che contribuì a fargli vincere il premio Nobel (1939). Le conoscenze acquisite lo portarono inoltre alla sintesi dei primi muschi sintetici macrociclici: exaltone (1924), civettone (1924), exaltolide (1928), globanone (1928), muscone (1933).[3] I muschi macrociclici risultano in genere facilmente biodegradabili e sono stati in seguito ampiamente sviluppati da altri ricercatori. A partire dagli anni 60 furono introdotte nuove procedure di sintesi che resero facilmente accessibili molte nuove fragranze di questa famiglia.[2] Alcuni muschi sintetici macrociclici di importanza commerciale sono raffigurati nelle figure seguenti.[1]
-

-
 Habanolide
Habanolide -
 Astratone
Astratone -
 Ambrettolide
Ambrettolide -
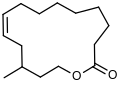 Nirvanolide
Nirvanolide
Muschi aliciclici
La ricerca di muschi sintetici a minor impatto ambientale ha portato alla nuova famiglia dei muschi aliciclici. Il primo rappresentante di questa tipologia è stato Helvetolide (1990), seguito pochi anni dopo da Romandolide (1998). Queste molecole in soluzione tendono ad assumere una conformazione simile a un anello macrociclico. Alcune altre fragranze appartenenti a questa tipologia sono sylkolide (2002) serenolide (2001) e edenolide (2004).[4]
-
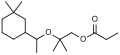
-
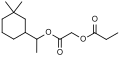
-
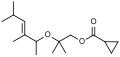 sylkolide
sylkolide -
 serenolide
serenolide -
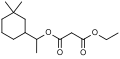 edenolide
edenolide
Altri
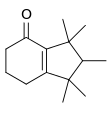
Ci sono inoltre muschi sintetici non direttamente inquadrabili nei gruppi precedenti. Alcuni dei più noti sono Cashmeran (1969), Moxalone (1983), Nebulone (2001) e Sinfonide (2012).
-
-
 Moxalone
Moxalone -
 Nebulone
Nebulone -
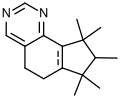 Sinfonide
Sinfonide
Note
Bibliografia
- (EN) N. Armanino, J. Charpentier, F. Flachsmann, A. Goeke e et al., What's Hot, What's Not: The Trends of the Past 20 Years in the Chemistry of Odorants, in Angew. Chem. Int. Ed., vol. 59, n. 39, 2020, pp. 16310–16344, DOI:10.1002/anie.202005719.
- (DE) A. Baur, Studien über den künstlichen Moschus, in Ber. Dtsch. Chem. Ges., vol. 24, n. 2, 1891, pp. 2832-2843, DOI:10.1002/cber.189102402106.
- (EN) O.R.P. David, Artificial Nitromusks, Stories of Chemists and Businessmen, in Eur. J. Org. Chem., vol. 2017, n. 1, 2017, pp. 4-13, DOI:10.1002/ejoc.201601249.
- (EN) O.R.P. David, A Chemical History of Polycyclic Musks, in Chem. Eur. J., vol. 26, n. 34, 2020, pp. 7537-7555, DOI:10.1002/chem.202000577.
- (EN) O.R.P. David e F. Doro, Industrial Fragrance Chemistry: A Brief Historical Perspective, in Eur. J. Org. Chem., vol. 26, n. 44, 2023, pp. e202300900, DOI:10.1002/ejoc.202300900.
- (EN) G. Rádis-Baptista, Do Synthetic Fragrances in Personal Care and Household Products Impact Indoor Air Quality and Pose Health Risks?, in J. Xenobiot., vol. 13, n. 1, 2023, pp. 121-131, DOI:10.3390/jox13010010.
- (EN) J. Regueiro, M. Llompart, C. Garcia-Jares e R. Cela, Development of a high-throughput method for the determination of organochlorinated compounds, nitromusks and pyrethroid insecticides in indoor dust, in J. Chromatogr. A, vol. 1174, n. 1-2, 2007, pp. 112-124, DOI:10.1016/j.chroma.2007.08.052.
- (EN) J. Regueiro, C. Garcia-Jares, M. Llompart, J. P. Lamas e R. Cela, Development of a method based on sorbent trapping followed by solid-phase microextraction for the determination of synthetic musks in indoor air, in J. Chromatogr. A, vol. 1216, n. 14, 2009, pp. 2805-2815, DOI:10.1016/j.chroma.2008.09.062.
- (EN) J. L. Reiner, C. M. Wong, K. F. Arcaro e K. Kannan, Synthetic Musk Fragrances in Human Milk from the United States, in Environ. Sci. Technol., vol. 41, n. 11, 2007, pp. 3815–3820, DOI:10.1021/es063088a.
- (EN) D. J. Rowe (a cura di), Chemistry and Technology of Flavors and Fragrances, Oxford, Blackwell, 2005, ISBN 1–4051–1450–9.
- (EN) S. A. Rubinfeld e R. G. Luthy, Nitromusk compounds in San Francisco Bay sediments, in Chemosphere, vol. 73, n. 6, 2008, pp. 873-879, DOI:10.1016/j.chemosphere.2008.07.042.
- (EN) C. Sommer, The Role of Musk and Musk Compounds in the Fragrance Industry, in G. G. Rimkus (a cura di), Synthetic Musk Fragrances in the Environment, Berlino, Springer, 2004, DOI:10.1007/b14173, ISBN 3-540-43706-1.
Altri progetti
 Portale Chimica
Portale Chimica Portale Moda
Portale Moda





































